IL15(インターロイキン-15)は多面作用性のサイトカインとして、活性化された単球、すなわちマクロファージ、表皮細胞、線維芽細胞、その他の細胞によって産生され、IL2と同様な生物学的活性を発揮し、T細胞、B細胞、NK細胞を活性化し、これらの細胞の増殖と生存機能を介在する機能をもっています。集萃薬康は、NCGマウスモデルでヒト化IL15遺伝子をノックインし、ヒト化NK細胞のコロニー形成と活性をサポートできる第2世代NCG系統NCG-hIL15を取得しました。
huHSC-NCG-hIL15はヒト造血幹細胞(CD34+HSC)をNCG-hIL15マウスに移植することで取得した人免疫系再構築モデルです。このモデルは機能性をもったT細胞とNK細胞を再構築したもので、生存周期が39週間以上で、腫瘍免疫治療薬の研究に利用できます。
huHSC-NCG-hIL15応用
l ヒト細胞、組織の移植に使われます。
l ヒト腫瘍を接種し、関連治療薬のスクリーニング、特にADCC作用に基づく薬力学的評価に使われます。
l ヒト造血系及び免疫系の研究に使われます。
業務詳細
NCG-hIL15マウス末梢血のヒトIL15発現レベル
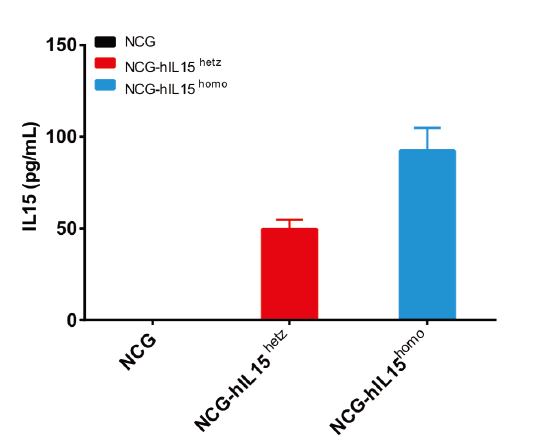
ヒトIL15の発現は、NCG-hIL15ヒト化マウスのヘテロ接合体とホモ接合体の両方で検出でき、ホモ接合体の発現レベルはヘテロ接合体より高いです。
2. huHSC-NCG-hIL15再構築効果の特定、T、NK細胞再構築
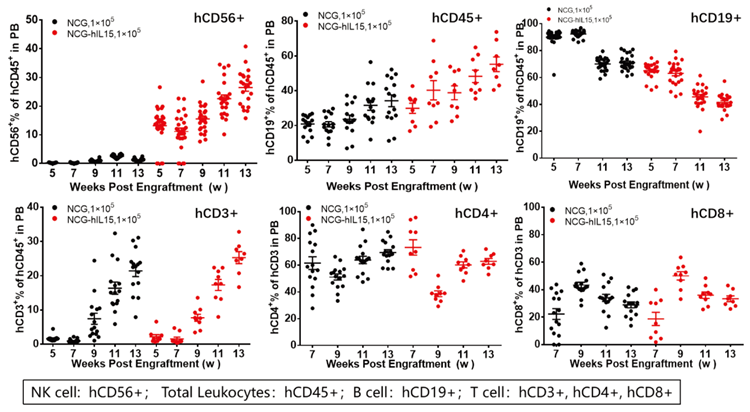
huHSC-NCG及びhuHSC-NCG-hIL15マウス末梢血での各免疫細胞の再構築レベル。huHSC-NCG及びhuHSC-NCG-hIL15マウスの末梢血を7、9、11、および13週目に採取し、フローサイトメトリーでhuHSC-NCGマウス及びhuHSC-NCG-hIL15マウスのヒト化過程を測定しました。測定指標はhCD45, hCD3, hCD19, hCD4, hCD8, hCD56です。免疫再構築過程では、5週間前後でhuHSC-NCG-hIL15マウス末梢血のhCD45+白血球レベルは20%以上に達し、その中で、hCD3+ T細胞レベルは徐々に増加し、かつhCD4+及びhCD8+ T細胞サブグループが分化されました。huHSC-NCGマウスに比べ、CD56+NK細胞の再構築レベルは有意に高かったです。
3. huHSC-NCG及びhuHSC-NCG-hIL15マウス末梢血でのNK細胞機能遺伝子発現の測定

huHSC-NCG及びhuHSC-NCG-hIL15マウス末梢血を13週目に採取し、フローサイトメトリーでhuHSC-NCGマウス及びhuHSC-NCG-hIL15マウス末梢血において再構築されたヒトNK細胞機能遺伝子発現状況を測定しました。測定指標はCD56、CD16、KIR3DL、NKG2Dです。huHSC-NCGに比べ、huHSC-NCG-hIL15マウスのヒトNK細胞再構築レベルは有意に高くなり、かつ、KIR3DL、NKG2D機能性タンパク質を発現できます。
4. huHSC-NCG-hIL15に基づくin vitro薬力学的実験
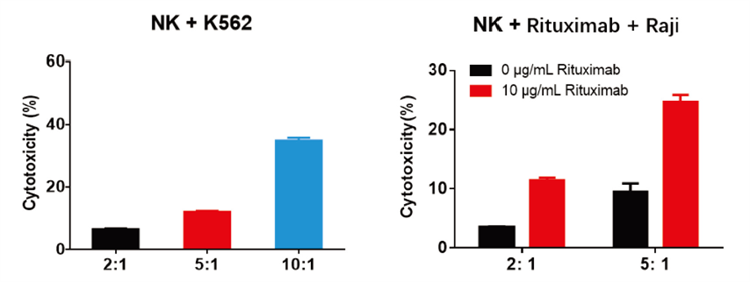
NCG-hIL15マウスにおける移植ヒト造血干細胞HSCの再構築NK細胞の死滅とADCC効果は
エフェクターと標的の比率によって高められ(NK:K562=2: 1,5: 1,10: 1)、NCG-hIL15ヒト化マウス再構築NK細胞はヒト慢性骨髄性白血病細胞K562に対する死滅率も高められます。エフェクターと標的の比率(NK:Raji=2: 1,5: 1)により、NCG-hIL15ヒト化マウス再構築NK細胞のRaji細胞に対する死滅率も高められます。0μg/mL及び10μg/mLのRituximab(標的CD20抗体,主に抗体依存性細胞に介在された細胞毒性作用ADCCで死滅するCD20+腫瘍細胞)を加えると、Rituximab抗体はNK細胞に介在されたADCC作用により、Raji細胞に対する死滅効果が更に高められます。
5. huHSC-NCG-hIL15に基づくin vivo薬力学的実験

対数増殖期のヒトリンパ腫細胞Raji細胞をhuHSC-NCG-hIL15マウスに皮下接種し、腫瘍増殖平均体積が約40-50 mm3になったときに、無作為にPBS群,Rituximab投与群及びBlincyto投与群に分け、対応の治療薬で治療を行いました。試験結果:Rituximab群(TGI=48.95%)及びBlincyto群(TGI=59.67%)はhuHSC-NCG-hIL15のRaji細胞担癌マウスの腫瘍増殖に対する抑制効果が認められました。