(BALB/c-hCD137, BALB/c-hPD1/hCD137, BALB/c-hPD1/hPDL1/hCD137, C57BL/6-hCD137, C57BL/6-hPD1/hCD137)
CD137(4-1BB,TNFRSF9)はI型膜貫通タンパク質として、腫瘍壊死因子受容体スーパーファミリーの一員です。活性化されたCD4+T、CD8+T細胞表面で発現し、CD137Lとの結合により、T細胞の共刺激シグナルを構成します[1]。CD137は主にT細胞の免疫応答に関与し、CD28と協力して、免疫の後期にT細胞の共刺激シグナルと生存シグナルを提供でき、免疫応答を維持し、免疫細胞のアポトーシスに抵抗し、抗原特異的免疫細胞のクリアランスを減らし、免疫記憶を強化することに重要な役割を果たします。CD137はNK細胞の増殖とIFNγ産生を刺激し[2]、サイトカイン産生とB7上方調節を促進することにより、DC活性化を介在します[3]。また、CD137は活性化誘発細胞死(activation-induced cell death,AICD)からT細胞を保護することができます[1]。さらに、CD137は腫瘍組織の血管壁、CD137Lはさまざまなヒト腫瘍組織細胞の表面に発現し、CD137 / CD137Lは腫瘍の微小環境において重要な役割を果たしています。
構築戦略:集萃薬康はBALB/c及びC57BL/6マウスのCD137遺伝子コード細胞外領域を対応のヒト遺伝子配列に置き換え、細胞内領域は完全なマウス配列を保持することで、単一ヒト化マウスBALB/c-hCD137とC57BL/6-hCD137,二重ヒト化マウスBALB/c-hPD1/hCD137とC57BL/6-hPD1/hCD137,三重ヒト化マウスBALB/c-hPD1/hPDL1/hCD137を含むCD137ヒト化マウスモデルを構築しました。CD137ヒト化マウスモデルはヒトCD137アゴニストの薬力学的評価及び安全性評価に利用できます。
1. BALB/c-hCD137:Urelumabの薬力学的実験
CT26.WT腫瘍細胞をBALB/c-hCD137マウスモデルに皮下接種した後、ヒトCD137抗体であるUrelumabの腫瘍抑制効果試験を実施しました。

左図:マウス腫瘍増殖グラフ 右図:マウス体重変化グラフ
![]() 対数増殖期の結腸癌細胞CT26.WTを5-8週齢のBALB/c-hCD137ヒト化マウスに皮下接種し、腫瘍増殖平均体積が約100 mm3になったときに、無作為にVehicle(対照)群,Urelumab群(n=6)に分け、対応の治療薬で治療を行いました。週に2回、計6回投与しました。データはMean±SEMで示されたものです。
対数増殖期の結腸癌細胞CT26.WTを5-8週齢のBALB/c-hCD137ヒト化マウスに皮下接種し、腫瘍増殖平均体積が約100 mm3になったときに、無作為にVehicle(対照)群,Urelumab群(n=6)に分け、対応の治療薬で治療を行いました。週に2回、計6回投与しました。データはMean±SEMで示されたものです。
試験結果:抗ヒトCD137抗体であるUrelumabは腫瘍増殖に対し非常に有意な抑制作用が認められました(TGI=64.26%)。
考察:BALB/c-hCD137マウスはヒトCD137抗体の薬力学的効果を評価するための理想的なモデルです。
2.C57BL/6-hCD137:Urelumab和Utomilumab類似体の薬力学的実験
MC38腫瘍細胞株をC57BL/6-hCD137マウスモデルに皮下接種した後、抗ヒCD137抗体であるUrelumab及びUtomilumab類似体の腫瘍抑制効果試験を実施しました。
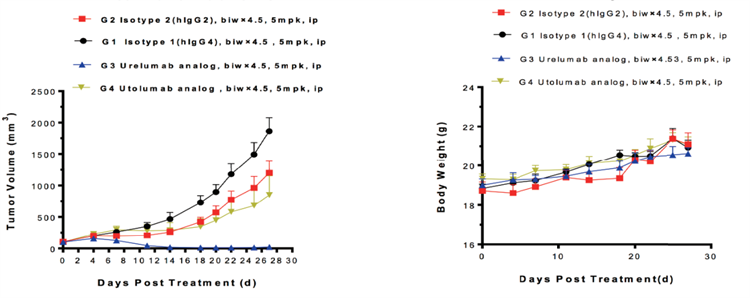
左図:マウス腫瘍増殖グラフ 右図:マウス体重変化グラフ
B6-hCD137マウスへのMC38皮下接種モデルに基づくin vivo薬力学的試験。マウス結腸癌細胞MC38をB6-hCD137ヒト化マウスに皮下移植し、腫瘍平均体積が約100 mm3になったときに、無作為に対照群と治療群(n=6)に分けました。データはMean±SEMで示されたものです。
試験結果:抗ヒトCD137抗体でであるUrelumabは腫瘍増殖に対し有意な抑制作用が認められたが(TGI=100%)、抗ヒトCD137抗体であるUtolumabは腫瘍増殖に対し、一部の腫瘍抑制作用しか認められず(TGI=47.67%)、薬力学的効果試験結果は臨床試験結果と一致しています。
考察:B6-hCD137マウスはヒトCD137抗体のin vivo薬力学的効果を評価するための効果的なツールです。
3. BALB/c-hPD1/hPDL1/hCD137:Urelumab類似体及びKeytrudayの薬力学的実験
CT26-hPDL1(Tg)-mPDL1(KO)腫瘍細胞をBALB/c-hPD1/hPDL1/hCD137マウスモデルに皮下接種した後、抗ヒトCD137抗体であるUrelumab類似体と抗ヒトPD1抗体の腫瘍抑制効果試験を実施しました。
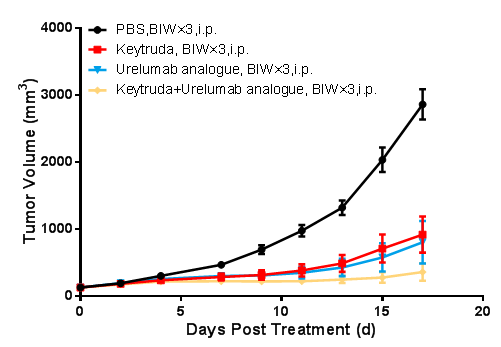
マウス腫瘍増殖グラフ
BALB/c-hPD1/hPDL1/hCD137マウスへのCT26-hPDL1(Tg)-mPDL1(KO)皮下接種モデルに基づくin vivo薬力学的試験。対数増殖期の結腸癌細胞CT26-hPDL1(Tg)-mPDL1(KO)を6-8週齢のBALB/c-hPD1/hPDL1/hCD137ヒト化マウスに皮下接種し、腫瘍増殖平均体積が約100 mm3になったときに、無作為にPBS群、Keytruda群、Urelumab analogue群及びKeytrudaとUrelumab analogue併用群 (n=8)に分け、対応の治療薬で治療を行いました。週に2回、計5回投与しました。データはMean±SEMで示されたものです。
試験結果:Keytruda群とUrelumab analogue単剤群の腫瘍増殖抑制率(TGI)はそれぞれ69.68%と72.21%で、KeytrudaとUrelumab analogue併用群のTGIは87.22%であり、各投与群はすべて腫瘍増殖に有意な抑制作用があり、かつ併用群の抑制作用がさらに効果的です。
考察:BALB/c-hPD1/hPDL1/hCD137マウスはヒトCD137抗体、PD-1/PD-L1抗体及び併用薬の抗腫瘍薬效作用の評価に利用できます。
4. C57BL/6-hPD1 /hCD137:Anti-CD137 Ab和Keytrudayの薬力学的実験
MC38腫瘍細胞株をB6-hPD1/hCD137マウスモデルに皮下接種した後、抗ヒトCD137抗体及び抗ヒトPD1抗体であるKEYTRUDA®(Pembrolizumab)の腫瘍抑制効果試験を実施しました。
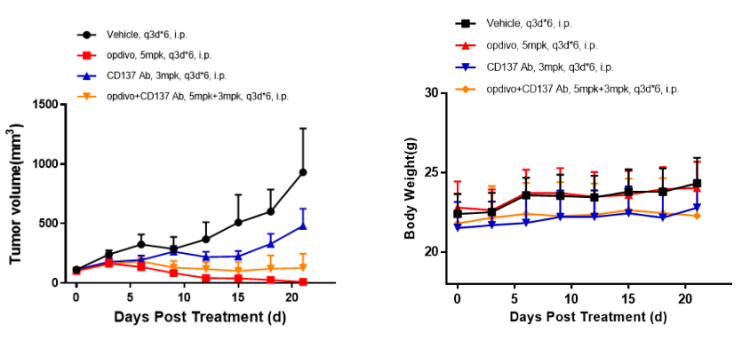
左図:マウス腫瘍増殖グラフ 右図:マウス体重変化グラフ
B6-hPD1/hCD137に基づくin vivo抗ヒトCD137抗体及び抗ヒトPD1抗体の薬力学的実験。対数増殖期の結腸癌細胞MC38を6-8週齢のB6-hPD1/hCD137ヒト化マウスに皮下接種し、腫瘍増殖平均体積が約100 mm3になったときに、無作為にVehicle(対照群,n=5),CD137 Ab 3mg/kg群(n=5),Opdivo 5mg/kg群(n=4),CD137 Ab 3mg/kg + Opdivo 5mg/kg群(併用群,n=5)に分けました。3日に1回、計6回投与しました。データはMean±SEMで示されたものです。
試験結果:CD137 AbとOpdivo併用群(TGI=86.2%)及びOpdivo 5mg/kg群(TGI=98.8%)は腫瘍増殖に対し有意な抑制効果が認められ、CD137 Ab 3mg/kg群は部分的に腫瘍増殖を抑制できます(TGI=48.3%)(左図)。4群のマウスの体重は有意に変化しませんでした(右図)。
考察:B6-hPD1/hCD137マウスは抗ヒトCD137抗体と抗ヒトPD1抗体併用効果を評価するための理想的な動物モデルです。
参考文献
[1] Cannons JL, et al. 4-1BB ligand induces cell division, sustains survival, and enhances effector function of CD4 and CD8 T cells with similar efficacy. J.Immunol. 2001; 167:1313‒1324.
[2] Wilcox RA, Tamada K, Strome SE, Chen L. Signaling through NK cell-associated CD137 promotes both helper function for CD8+ cytolytic T cells and responsiveness to IL-2 but not cytolytic activity. J. Immunol. 2002; 169:4230‒4236.
[3] Wilcox RA, et al. Cutting edge: expression of functional CD137 receptor by dendritic cells. J. Immunol. 2002;168:4262‒4267.