(BALB/c-hTIGIT, BALB/c-hPD1/hTIGIT, , BALB/c-hPD1/hPDL1/hTIGIT 、C57BL/6-hTIGIT, C57BL/6-hPD1/hTIGIT)
TIGIT (T cell immunoglobulin and ITIM domain)はⅠ型膜貫通タンパク質として、細胞外領域に一つの免疫グロブリン構造領域、細胞内にITIM構造領域が含まれ、主にT-cellとNK-cell表面に発現します。
メカニズム研究により、TIGITの欠損は、MOGペプチドで免疫した後のT細胞応答の増強に繋がり、TIGITがT細胞の抑制性受容体であることを明らかにされました。
現在、TIGITの細胞に対する抑制機能は2つの方式で実現されたものだと考えられます。一つは、TIGITが直接に細胞自体に機能し、TCRα鎖を下方調節することによって媒介シグナル伝達を弱めることで、細胞の活性化を抑制するもので[1]、もう一つは、APC上のPVRリガンドの下流シグナル伝達経路をトリガーし、シグナル伝達分子であるERKのリン酸化レベルを高め、APCからの抗炎症因子IL-10の分泌を強化し、IL-10が更に細胞に作用することでT細胞応答を阻害するものです[2]。GenentechのTIGIT抗体であるMTIG7192Aの臨床試験結果によると、単剤またはPD-L1抗体であるAtezolizumabとの併用により、進行性または転移性腫瘍を治療できます。
構築戦略:集萃薬康はBALB/c及びC57BL/6マウスのTIGIT遺伝子にコード化された細胞外領域を対応のヒトセグメントに置き換え、マウスのTIGITタンパク質の細胞内部分を完全に保持することで、単一ヒト化マウスBALB/c-hTIGIT及びC57BL/6-hTIGIT,二重ヒト化マウスBALB/c-hPD1/hTIGIT及びC57BL/6-hPD1/hTIGIT,三重ヒト化マウスBALB/c-hPD1/hPDL1/hTIGITを含むTIGITヒト化マウスモデルを構築しました。TIGITヒト化マウスモデルはヒトTIGIT阻害剤の薬力学的効果を評価するための理想的な動物モデルです。
1. BALB/c-hTIGIT/及びB6-hTIGITのin vivo薬力学的評価
それぞれCT26.WT腫瘍細胞株をBALB/c-hTIGITマウスモデルに、MC38腫瘍細胞株をB6-hTIGITマウスモデルに皮下接種した後、抗ヒトTIGIT抗体の腫瘍抑制効果試験を実施しました。

左図:BALB/c-hTIGITのin vivo薬力学的効果;右図:B6-hTIGITのin vivo薬力学的効果
BALB/c-hTIGITとB6-hTIGITに基づくのin vivo薬力学的効果比較試験。対数増殖期のマウス結腸癌細胞CT26.WTとMC38をそれぞれBALB/c-hTIGITとB6-hTIGITマウスに皮下接種し、腫瘍増殖平均体積が約80-120 mm3になったときに、無作為に対照群及びanti-hTIGIT単剤群(n=10)に分け、週に2回、計6回投与しました。データはMean±SEMで示されたものです。
試験結果:BALB/c-hTIGITマウスにCT26.WT腫瘍を接種し、抗ヒトTIGIT抗体で治療した場合、良好な抗腫瘍効果(TGI=40.26%)が認められたが、B6-hTIGITマウスにMC38腫瘍を接種し、抗ヒトTIGIT抗体で治療した場合、腫瘍抑制効果(TGI=12.03%)が認められませんでした。
考察:MC38細胞を接種したB6-hTIGITマウスモデルに比べ、抗ヒトTIGIT抗体はCT26.WT細胞を接種したBALB/c-hTIGITマウスモデルに対するin vivo薬力学的効果が高いため、BALB/c-hTIGITマウスモデルは抗ヒトTIGITの薬力学的効果を評価するための理想的なモデルだと考えられます。
2. BALB/c-hPD1/hTIGIT及びB6-hPD1/hTIGITのin vivo薬力学的効果
それぞれCT26.WT腫瘍細胞株をBALB/c-hPD1/hTIGITマウスモデルに、MC38腫瘍細胞株をB6-hPD1/hTIGITマウスモデルに皮下接種した後、抗ヒトTIGIT抗体の腫瘍抑制効果試験を実施しました。
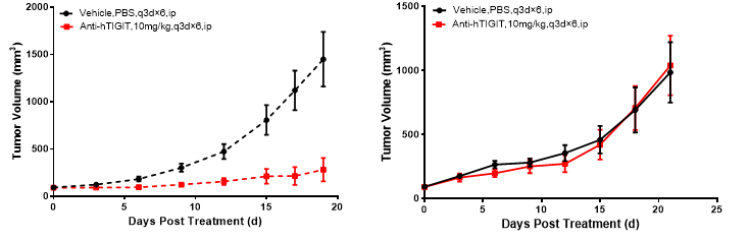
左図:BALB/c-hPD1/hTIGITのin vivo薬力学的効果;右図:B6- hPD1/hTIGITのin vivo薬力学的効果
BALB/c-hPD1/hTIGITとB6-hPD1/hTIGITに基づくのin vivo薬力学的効果比較試験。対数増殖期のマウス結腸癌細胞CT26.WTとMC38をそれぞれBALB/c-hPD1/hTIGITとB6-hPD1/hTIGITに皮下接種し、腫瘍増殖平均体積が約80-120 mm3になったときに、無作為に対照群とAnti-hTIGIT単剤群(n=6)に分け、週に2回、計6回投与しました。データはMean±SEMで示されたものです。
試験結果:試験結果:BALB/c-hPD1/hTIGITマウスにCT26.WT腫瘍を接種し、抗ヒトTIGIT抗体で治療した場合、良好な抗腫瘍効果(TGI=79%)が認められましたが、B6-hPD1/hTIGITマウスにMC38腫瘍を接種し、抗ヒトTIGIT抗体で治療した場合、腫瘍抑制効果が認められませんでした。したがって、MC38細胞を接種したB6-hPD1/hTIGITマウスモデルに比べ、抗ヒトTIGIT抗体のCT26.WT細胞を接種したBALB/c-hPD1/hTIGITマウスモデルに対するin vivo薬力学的効果は高いです。
考察:BALB/c-hPD1/hTIGITマウスモデルは抗ヒトTIGITの薬力学的効果を評価するための理想的なモデルです。
1. BALB/c-hPD1/hTIGIT:KeytrudaとTriagolumab、M Triagolumab抗体の抗腫瘍効果の評価
CT26.WT腫瘍細胞株をBALB/c-hPD1/hTIGITマウスモデルに皮下接種した後、抗ヒトPD1抗体(keytruda)、Triagolumab及びM Triagolumabの腫瘍抑制効果試験を実施しました。

BALB/c-hPD1/hTIGITのin vivo薬力学的効果
(データは第三者の共同検証による)
BALB/c-hPD1/hTIGITマウスに基づく薬力学的実験。対数増殖期のマウス結腸癌細胞CT26.WTをBALB/c-hPD1/hTIGITマウスに皮下接種し、腫瘍増殖平均体積が約80-120 mm3になったときに、無作為にHuman IgG1群,Keytruda単剤群、Tiragolumab単剤群、M Tiragolumab単剤群及びKeytruda+ Tiragolumab併用群(n=8)に分け、週に2回、計6回投与しました。データはMean±SEMで示されたものです。
試験結果:Keytruda治療群とTiragolumab治療群の腫瘍増殖抑制率(TGI)はそれぞれ56.79%、75.34%で、腫瘍増殖に対するある程度の抑制作用が認められました。Keytruda+ Tiragolumab併用群はより高い腫瘍抑制作用が認められ、TGIは88.94%でした。M TiragolumabはTiragolumabのFc部分を突然変異することで、Tiragolumab介在のADCC(抗体依存性細胞に介在された細胞毒性作用)をなくしたため、腫瘍増殖を効果的に抑制できません(TGI=10.04%)。
考察:BALB/c-hPD1/hTIGITマウスはヒトPD1、TIGIT抗体及び併用薬をスクリーニング及び評価するための理想的な動物モデルであり、抗体薬であるADCCの作用評価にも利用できます。
参考文献
[1] Joller, Nicole, et al. "Cutting edge: TIGIT has T cell-intrinsic inhibitory functions." The Journal of Immunology 186.3 (2011): 1338-1342.
[2] Stanietsky, Noa, et al. "The interaction of TIGIT with PVR and PVRL2 inhibits human NK cell cytotoxicity." Proceedings of the National Academy of Sciences 106.42 (2009): 17858-17863.