银屑病俗称牛皮癣,是一种由遗传、免疫、感染等多种因素诱发的慢性自身免疫性皮肤疾病[1]。各国公布的银屑病患病率在0.09%至11.43%之间,世界范围内约有1.25亿银屑病患者。
银屑病发病机制
先天性和适应性免疫细胞共同促成了银屑病的病理过程。感染和物理损伤等触发因素刺激树突状细胞(DCs)释放促炎因子(IL-23、TNF-α和IL-12)。这些细胞因子激活IL-23和/或IL-22通路,诱导Th17和/或Th22细胞分化,导致大量银屑病细胞因子的产生,如TNF-α、IFN-γ、IL-17和IL-22,它们作用于角质形成细胞,放大银屑病炎症。此外,皮肤浸润细胞,如γδT细胞,通过产生IL-17参与疾病的发展,Treg细胞和Th17/Treg平衡也在银屑病的发病过程中发挥重要作用[2]。人们对银屑病发病机制的理解,推动了靶点药物的发现和应用。动物模型在这个过程中做出了重要贡献。

图一.银屑病中发挥作用的免疫细胞和药物靶点[2]
几种常见银屑病动物模型技术
人们一开始无法在实验动物身上观察到银屑病的发生,银屑病动物模型的缺乏使得早期的科学研究在很大程度上受到阻碍。一个好的银屑病模型需要反映银屑病关键的组织学特征,重现银屑病的免疫学特征,并且对已被证明有效的银屑病疗法有响应[3]。目前市面上已有多种银屑病动物模型,包括自发表型模型、基因编辑模型、异源移植模型和诱导类模型,接下来小编将为大家介绍几种银屑病领域最常用的动物模型。
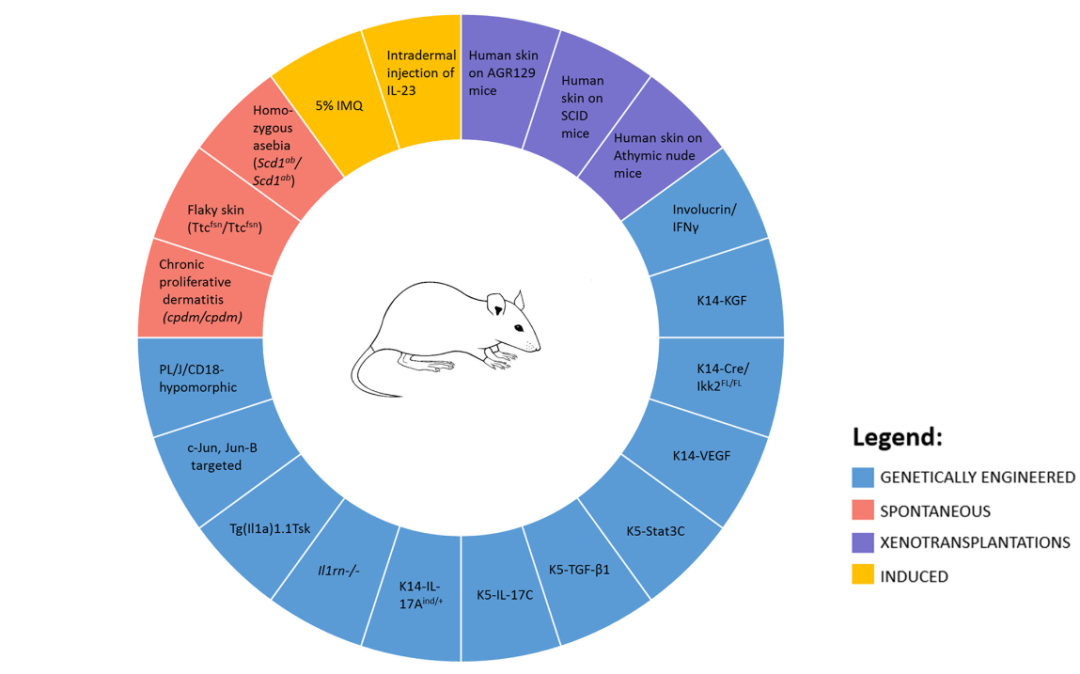
图二.银屑病小鼠模型[4]
四种银屑病领域最常用的动物模型:
一、03K14-IL-17A银屑病小鼠
IL-17细胞因子家族在宿主对病原体的反应中发挥重要作用。银屑病患者血清IL-17水平明显升高,其中IL-17A和IL-17C是升高最多的家族成员。IL17A中和抗体也能够有效缓解银屑病症状。因此,制作一个IL17A基因编辑小鼠是有可能复刻出人类银屑病的特征的。研究人员通过将IL-17A转基因小鼠与K14-Cre鼠杂交产生K14-IL-17A小鼠。这些老鼠出现明显的皮肤炎症,具有人类银屑病的许多标志性特征,包括效应T细胞的真皮浸润、角化过度、中性粒细胞微脓肿的形成。由于该模型在免疫学上与人类银屑病相似,因此在科学研究被广泛使用[5]。

图三、K14-IL-17A小鼠银屑病表型[5]
集萃银屑病模型推荐
品系编号 | 品系简称 | 品系简介 |
人类角蛋白KRT14启动子驱动的Cre工具鼠 | ||
条件性插入人源IL-17A,需和Cre工具鼠配繁后使用 |
二、IMQ诱导银屑病小鼠模型
咪喹莫特(IMQ)是Toll样受体(TLRs)的配体,TLRs分布于巨噬细胞、单核细胞和浆细胞样树突细胞(pDC)上。因此,IMQ能够强烈激活免疫系统(例如,增强Th1反应或增加朗格汉斯细胞迁移)。每日使用IMQ涂抹近交系小鼠(如BALB/c)背部或耳部的皮肤,可诱导形成类似银屑病斑块的皮肤病变。这些变化伴随着表皮增殖增加、红斑、血管改变和角化细胞分化受损(由表皮中性粒细胞积累引起)。大量CD4+T细胞、CD11c+树突状细胞和pDC涌入皮肤。更重要的是,IMQ能够诱导IL-17A、IL-17F和IL-23基因的表达[4]。IMQ诱导银屑病小鼠模型,具有成本低、周期短的优势,因此是目前最常用的一种银屑病模型。
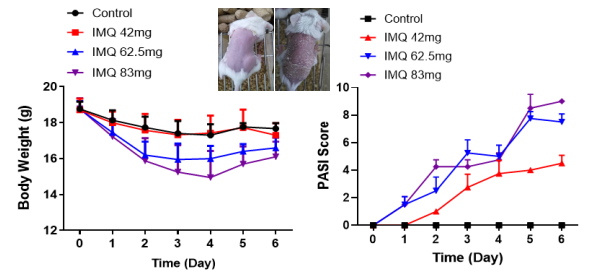
图四.IMQ诱导银屑病模型
IL-23/IL-17炎症轴在银屑病的发生发展中起到关键作用。银屑病的三大病理改变:炎症细胞浸润、新生血管形成以及角质形成细胞过度增殖,在K14-IL-17A模型和IMQ诱导模型中均可得到良好体现。因此,以上两种模型均是比较经典的银屑病小鼠模型。
三、基因人源化小鼠
抗体药具有起效快、副作用小的的优势,银屑病抗体药纳入医保后,使用量更是大幅提升。然而,抗体药与靶标的结合高度特异。临床有效的抗体药由于种属差异,在近交系小鼠上可能出现治疗无效的情况。基因人源化小鼠则能够解决这一困难。这类小鼠不一定表现出疾病特点,例如BALB/c-hIL17A小鼠本身不会产生银屑病,需要配合IMQ诱导造模,才能开展IL17A抗体药效实验。基因人源化小鼠被大量用于银屑病及其他自身免疫性疾病的临床前体内药效评价。
四、部分自免靶点基因人源化模型
以上仅仅介绍了一些在银屑病研究过程中较为常见的小鼠模型,在人类与疾病长期战斗的过程中,更多的动物模型作出了重要贡献,人类健康来之不易。
参考文献:
[1] Boehncke WH, Schön MP. Psoriasis. Lancet. 2015 Sep 5;386(9997):983-94.
[2] Hu P, Wang M, Gao H, Zheng A, Li J, Mu D, Tong J. The Role of Helper T Cells in Psoriasis. Front Immunol. 2021 Dec 15;12:788940.
[3] Gudjonsson JE, Johnston A, Dyson M, Valdimarsson H, Elder JT. Mouse models of psoriasis. J Invest Dermatol. 2007 Jun;127(6):1292-308.
[4] Bocheńska K, Smolińska E, Moskot M, et al. Jakóbkiewicz-Banecka J, Gabig-Cimińska M. Models in the Research Process of Psoriasis. Int J Mol Sci. 2017 Nov 24;18(12):2514.
[5] Croxford AL, Karbach S, Kurschus FC, et al. IL-6 regulates neutrophil microabscess formation in IL-17A-driven psoriasiform lesions. J Invest Dermatol. 2014 Mar;134(3):728-735.