人源PBMC(Peripheral Blood Mononuclear Cells)异体移植后的移植物抗宿主病(Graft-versus-Host Disease,GvHD)是一种严重的并发症,造成了PBM C移植后的小鼠出现严重的GvHD疾病并影响药效观测。因此,开发合适的模型来研究GvHD的发病机制、探索新的治疗策略以及评估抗体药物的疗效和安全性显得尤为重要。
集萃药康开发了NCG-MHC-dKO小鼠模型,该模型在缓解人源PBMC异体移植GvHD的同时,保持了IgG抗体的正常半衰期,并可以较好用于CD3 T细胞功能及抗体药物研究。本文将介绍该模型的特点、优势以及其在GvHD研究和免疫治疗领域的应用前景。
NCG-MHC-dKO小鼠模型是将NCG小鼠和MHC I类(H2k1,H2d1)和MHC II(H2Ab1)类缺失小鼠(MHC-dKO)的特性结合而构建的。NCG小鼠缺乏T、B和NK细胞,使其成为接受异体免疫细胞移植的理想宿主。而MHC-dKO小鼠则具有缺乏MHC I类和MHCII类表达的特点。通过将这两个特性结合成功地构建了NCG-MHC-dKO小鼠模型。
NCG-MHC-dKO小鼠在人源PBMC异体移植后显示出较低的GvHD发生率和严重程度。这是由于异体免疫细胞对于NCG-MHC-dKO小鼠的免疫系统的攻击能力较弱,从而减轻了GvHD引起的组织损伤,并且显著延长了NCG-MHC-dKO小鼠的生存期。该模型为研究GvHD的发病机制、寻找新的治疗策略以及评估药物疗效提供了有力的工具。

图1.NCG-MHC-dKO小鼠接种人源PBMC后的GvHD评分(左)和生存期(右)
NCG和NCG-MHC-dKO小鼠都移植2x107个人源PBMC细胞。结果发现与NCG小鼠相比,NCG-MHC-dKO小鼠表现出的GvHD症状更轻且具有更长的生存周期。
对IgG半衰期的影响:
值得注意的是,NCG-MHC-dKO小鼠模型保持了IgG抗体的正常半衰期。这一特点非常重要,因为IgG抗体在免疫治疗中起着重要的作用。保持正常的IgG抗体半衰期使得该模型能够更准确地评估抗体药物的疗效,为抗肿瘤免疫治疗的开发提供了可靠的平台。
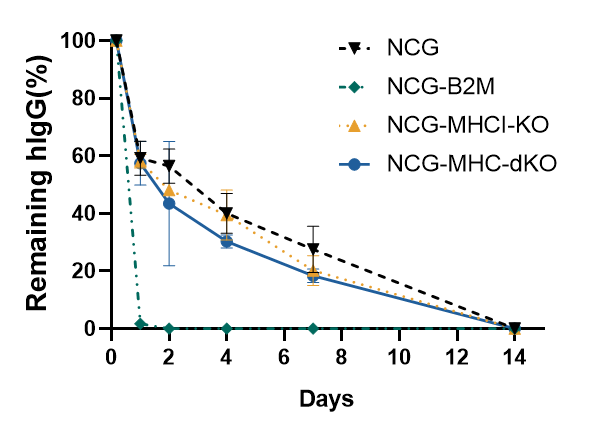
图2.NCG-MHC-dKO小鼠中人源IgG的半衰期
与NCG小鼠相比,NCG-B2M小鼠的人hIgG清除速度更快,而NCG-MHC-dKO小鼠的hIgG半衰期与NCG小鼠相似。
CD3 T细胞功能及抗体药物研究:
通过移植人源PBMC,NCG-MHC-dKO小鼠模型为研究CD3 T细胞的激活、增殖和功能提供了独特的机会。研究人员可以利用该模型评估不同CD3 T细胞亚群的功能,进一步探索其在GvHD发展中的作用,并为新的免疫治疗策略的开发提供重要的信息。此外,NCG-MHC-dKO小鼠模型还可用于评估CD3 T细胞功能抗体药物的疗效和安全性,为抗肿瘤免疫治疗的研究和开发提供了有力的支持。
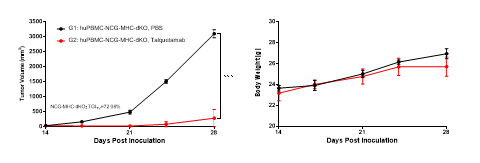
图3 Talquetamab在人源PBMC重建后的NCG-MHC-dKO模型中药效评价
Talquetamab能显著抑制NCG-MHC-dKO小鼠体内的肿瘤生长,并且治疗期间小鼠体重及状态稳定,说明NCG-MHC-dKO模型是评价CD3双抗药物的理想模型。

图4.Tecentriq在人源PBMC重建后的NCG-MHC-dKO模型中药效评价
Tecentriq(PDL1抑制剂)。从用药开始的30天内监测体重和肿瘤的测量。结果发现Tecentriq能显著抑制NCG-MHC-dKO小鼠体内的MDA-MB-231肿瘤生长。
结论:
NCG-MHC-dKO小鼠模型作为一种新的实验工具,展示了在缓解人源PBMC异体移植GvHD、保持IgG抗体半衰期以及研究CD3T细胞功能及抗体药物方面的潜力。该模型为GvHD的研究提供了新的途径,并为免疫治疗策略的发展提供了重要的支持。进一步的研究和应用将进一步揭示该模型的潜力和临床价值。
参考文献:
[1]Pearson T, et al. (2008). Specificity and effector mechanisms of human neutrophil defensins in antimicrobial immunity. Blood, 111(1): 8-15.
[2]Shultz LD, et al. (2012). Humanized mice for immune system investigation: progress, promise and challenges. Nat Rev Immunol, 12(11): 786-798.
[3]Ito M, et al. (2018). NOD/SCID/γcnull mouse: an excellent recipient mouse model for engraftment of human cells. Blood Cells Mol Dis, 70: 27-30.
[4]Smith DR, et al. (2020). NCG-MHC-dKO mice as a model for graft-versus-host disease and immune reconstitution. J Immunol Methods, 485: 112824.
[5]Mitchell JP, et al. (2019). Evaluation of CD3-targeted bispecific antibodies for efficient redirection of T cells to tumor cells. J Immunother Cancer, 7(1): 98.