帕金森病(Parkinson’s disease,PD 老年痴呆)是全球第二大神经退行性疾病,由于其迁延不愈的特点,被称为“不死的癌症”,多发于中老年人群。PD主要临床行为学特征包括静止性震颤、强直、运动迟缓和步态异常(如图一所示),临床病理特征主要表现为:黑质多巴胺能神经元的退化,纹状体多巴胺分泌减少和路易小体的形成[1]。
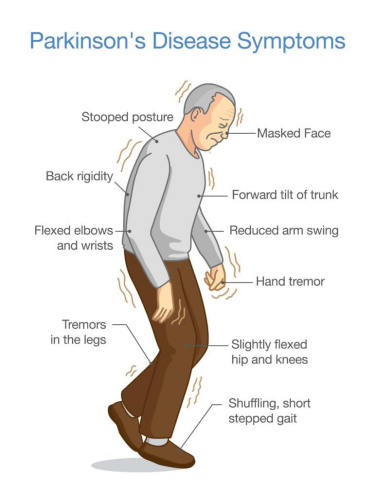
图一:帕金森病行为学症状
(图片来源:Possible Skin Test for Detecting Parkinson's Disease - Premier Neurology & Wellness Center (premierneurologycenter.com))
帕金森发病原理和发病机制
PD的发病机制极为复杂,具体病因尚未明确。目前认为主要和年龄、环境及基因因素相关。虽然年龄因素在PD中的作用已得到证实,但近年来呈现年轻化的趋势,经研究证实,这些患者体内的某些基因发生了突变或缺失,因此又被称为家族性PD。目前已经报道的PD相关基因有十多个,其中最常见的为LRRK2(亮氨酸重复激酶2)、SNCA(α-突触核蛋白)、PINK1、DJ-1、parkin等基因[2]。
1、 SNCA是最早发现的与帕金森病存在关联的基因之一
其中, SNCA是最早发现的与帕金森病存在关联的基因之一,也是揭示帕金森病发病机理的最有希望的靶点之一。SNCA编码的α-突触核蛋白(α-Synuclein, α-Syn)是一种在中枢神经系统突触前及核周表达的可溶性蛋白质,对突触可塑性、囊泡动力学和多巴胺合成具有潜在作用。病理性的α-Syn 生理状态的α-Syn为无序单体或螺旋折叠的四聚体,病理状态下为聚合状态,即毒性α-突触核蛋白,与路易小体的形成及多巴胺能神经元的死亡密切相关。在帕金森病中,这些包涵体主要分布于延髓、嗅球、蓝斑、黑质,并在较小程度上分布于皮质的各个区域。编码α-突触核蛋白的基因SNCA具有三个主要基因突变位点:A53T(Ala-Thr),A30P(Ala-Pro)和E46K(Glu-Lys)。这些突变都可以破坏蛋白原有分子空间结构和稳定性,致使α-突触核蛋白无法正常降解,异常聚集形成淀粉样结构(纤维、路易小体),从而引起神经元变性。
2、线粒体功能障碍相关因素也会导致PD的发生
除了基因突变,线粒体功能障碍相关因素也会导致PD的发生。线粒体DNA(mtDNA) 编码呼吸链的 13 个关键亚基, 被认为对线粒体生物发生至关重要。有报道表明神经毒素可通过阻断 mtDNA 功能实现呼吸链复合物 I 功能的有效破坏,进而导致中脑多巴胺能神经元功能丧失。在哺乳动物中,Tfam(线粒体转录因子 A)蛋白是维持 mtDNA 所必需的,它通过直接结合和包裹 mtDNA 来调节 mtDNA 的拷贝数。此外,Tfam 对于 mtDNA 启动子的转录起始也是绝对必需的,决定了线粒体 DNA 的转录起始。在多巴胺能神经元中特异性敲除 Tfam 后会导致线粒体 DNA 缺失,从而通过影响电子呼吸链导致多巴胺能神经元功能缺损,诱导PD相关疾病表型。
“困难重重”的帕金森疾病PD药物研发之路
截至目前,FDA批准的治疗PD药物约有25~30个(如图二所示),主要包括复方左旋多巴、多巴胺受体激动剂(DAs)、单胺氧化酶 B 型抑制剂(MAO-BI)、儿茶酚-O-甲基转移酶抑制剂(COMTI)、抗胆碱能药、金刚烷胺六大类。其中,复方左旋多巴是PD治疗中最常用的一种药物,也是帕金森病药物治疗中最有效的对症治疗药物。左旋多巴透过血脑屏障后,在脑内多巴脱羧酶的作用下,转化为多巴胺,通过直接补充脑内多巴胺神经递质从而发挥药理作用,尽管药效良好,但仍无法阻止PD疾病的进展,达到根治效果。
从1949年首款用于治疗PD的药物苯海索上市以来,人们对帕金森病的神经生物学机制、遗传及环境因素有了更加深入的了解,但帕金森病的新药研发之路还是困难重重,可用的生物标志物、良好的药物靶点及遗传基础等因素的探索缺乏均给药物研发带来了阻碍。因此,合适的疾病小鼠模型是推动PD机制研究和新药开发不可或缺的工具。
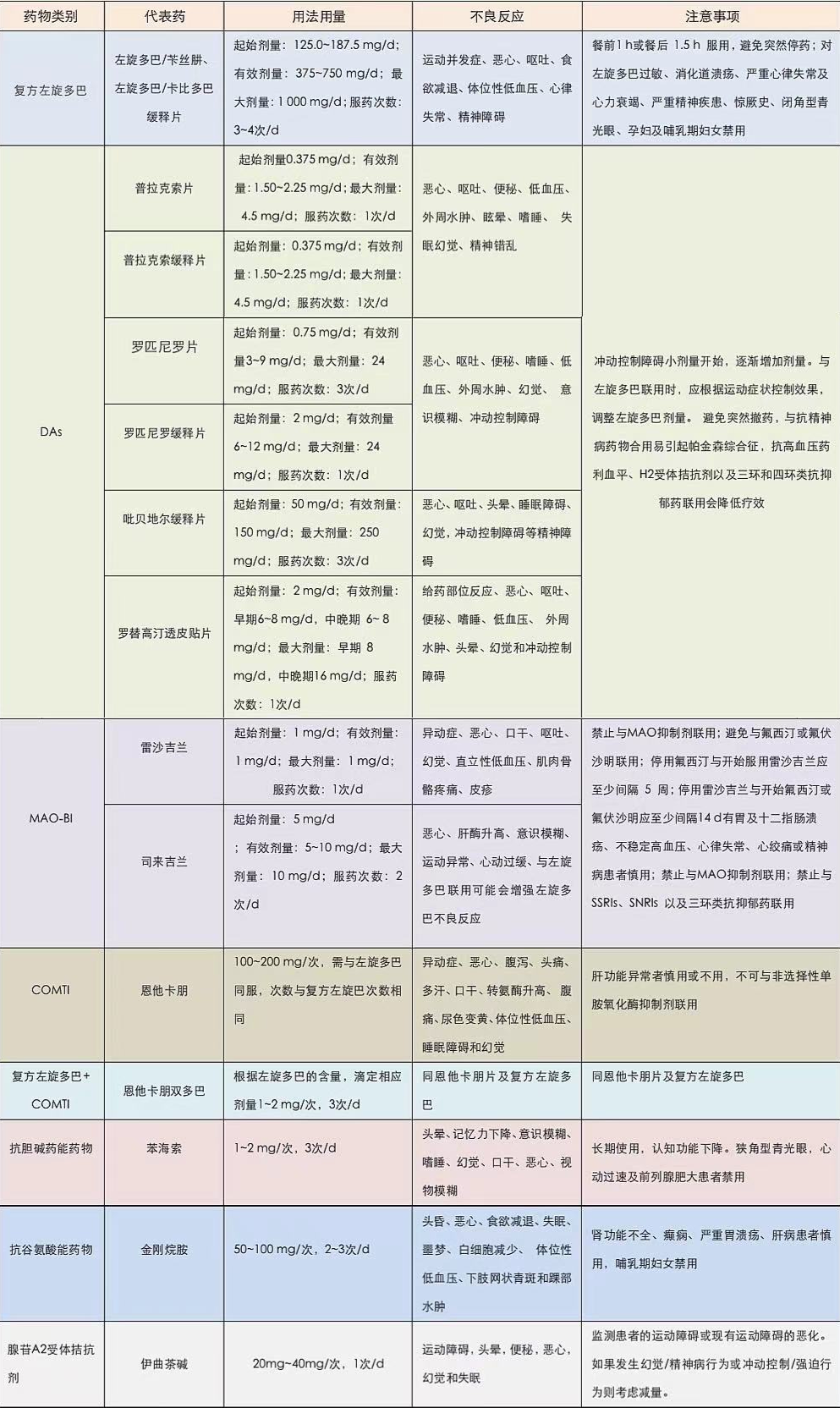
图二:帕金森治疗药物汇总
(图片来源:一文读懂:帕金森病药物治疗 - 丁香园 (dxy.cn))
帕金森(老年痴呆)小鼠模型——临床前研究好助手
集萃药康针对α-突触核蛋白异常聚集和线粒体功能异常机制分别构建了B6-hSNCA A53T及B6-Tfam-flox/Slc6a3-Cre模型,均可用于帕金森病治疗药物的筛选、安全性评价及发病机制研究。
帕金森(老年痴呆)小鼠模型品类一:B6-hSNCA A53T模型数据展示
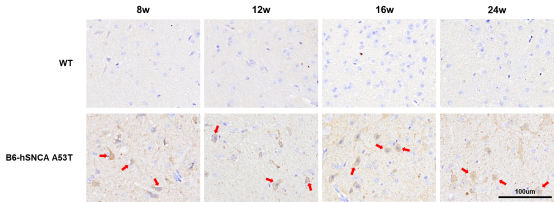
图三:B6-hSNCA A53T小鼠α-Syn聚集检测
B6-hSNCA A53T小鼠8周龄开始中脑及脑桥区域开始出现α-Syn蛋白胞质内聚集。
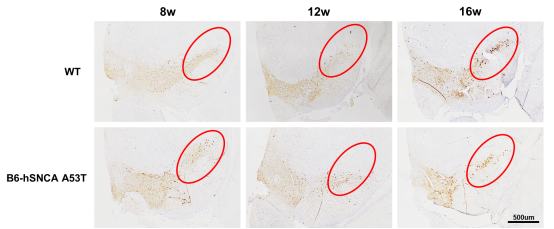
图四:B6-hSNCA A53T小鼠TH+神经元检测。
B6-hSNCA A53T小鼠16周龄开始SN和VTA区域出现TH+神经元减少的趋势。
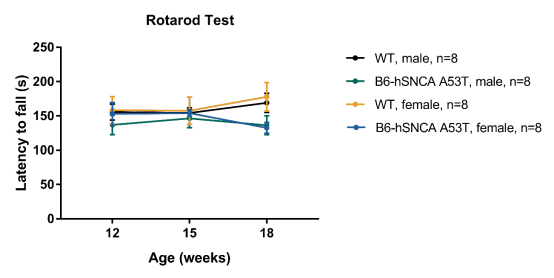
图五:B6-hSNCA A53T小鼠疲劳旋转棒测试
B6-hSNCA A53T小鼠在棒运动时间尚未表现出显著差异。
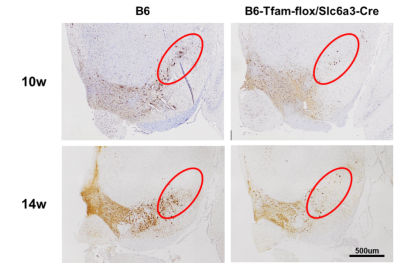
图六:B6-Tfam-flox/Slc6a3-Cre小鼠TH+神经元检测
10周龄开始B6-Tfam-flox/Slc6a3-Cre小鼠黑质区域TH+神经元减少,14周龄时显著少于B6对照小鼠。
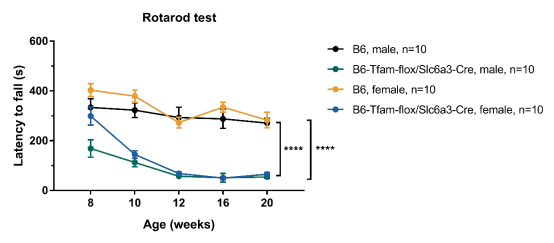
图七:B6-Tfam-flox/Slc6a3-Cre小鼠疲劳旋转棒测试
8周龄开始 B6-Tfam-flox/Slc6a3-Cre小鼠在棒运动时间开始降低,显著低于B6对照小鼠,且呈现年龄依赖性。
参考文献:
1.S.L. Kowal, T.M. Dall, R. Chakrabarti, M.V. Storm, A. Jain, The current and projected economic burden of Parkinson's disease in the United States, Mov Disord 28(3) (2013) 311-8.
2.帕金森病药物研发逐渐升温,以岭、绿叶、康缘谁能率先破局?_腾讯新闻 (qq.com)
3.2022年度帕金森患者疾病诊疗及生活质量报告_中国_病程_诊疗 (sohu.com)
4.K.A. Conway, J.C. Rochet, R.M. Bieganski, P.T. Lansbury, Jr., Kinetic stabilization of the alpha-synuclein protofibril by a dopamine-alpha-synuclein adduct, Science 294(5545) (2001) 1346.
5.科学网—科研资讯 | Front. Cell Dev. 帕金森病中的线粒体功能障碍 - Frontiers开放获取的博文 (sciencenet.cn)
6.一文读懂:帕金森病药物治疗 - 丁香园 (dxy.cn)