根据《2020中国心血管健康与疾病报告》数据显示,我国心血管病死亡占我国城乡居民总死亡原因的首位,农村为46.66%,城市为43.81%,并且中国城乡居民心血管死亡率近年来呈现持续上升的趋势。因此心血管疾病的预防和更好治疗药物的开发不容忽视。而高血脂症(高胆固醇血症、高甘油三脂血症或两者兼具)就是引发心血管疾病的一个重要因素,并且其与糖尿病、脂肪肝、肾脏疾病等关系密切。
胆固醇运输
人们从食物中摄取和自身合成来源的胆固醇在血液中的运输依赖于脂蛋白,细胞通过其表面的低密度脂蛋白受体(LDLR)与胞外的低密度脂蛋白(LDL)结合,并介导内化作用形成包含有LDL的胞内体,最终与溶酶体融合降解LDL,控制血液中“坏”胆固醇LDL-C水平,而LDLR则会返回细胞表面去结合更多血液中的LDL颗粒,进一步降低血液中LDL-C的水平[1-2]。
胆固醇调节因子——PCSK9
Proprotein Convertase Subtilisin/Kexin type 9 (PCSK9) 是体内胆固醇代谢途径中一种重要的调节因子,它被分泌到胞外后与LDLR结合形成复合物,再发生内化作用进入胞内被降解,PCSK9干扰LDLR的再循环,降低了肝脏从血液中清除LDL-C能力。人类PCSK9功能获得性突变与家族性高血脂症相关,携带PCSK9功能缺失性突变的人群其LDL-C水平较常人低15~28%,相应的心血管疾病的发病率也较正常人群减少50%以上[3-6]。同样在小鼠体内过表达和敲除PCSK9分别会下调和上调LDLR的表达水平,造成这两种小鼠出现高血脂症和低血脂症的表型[7-8]。因此PCSK9是体内胆固醇代谢途径中一种重要的调节因子,抑制其表达水平或活性能显著降低血液中LDL-C的水平,是进行降脂药物开发的有效靶点。

PCSK9靶向药物研发现状
目前,已有多家国内外药企在PCSK9靶点布局了新药研发管线。其中,赛诺菲的PCSK9抑制剂阿利西尤单抗Alirocumab和安进的依洛尤单抗Evolocumab两款抗体药已获批,在降低LDL-C水平方面均表现出了惊人的效果。更值得一提的是在2020年,诺华与Alnylam联合研发的PCSK9小干扰RNA(siRNA,Small Interfering RNA Drug)降胆固醇药物inclisiran获批,它能特异性的切割编码PCSK9的mRNA,在源头上减少了PCSK9的合成从而达到降低血液LDL-C水平的目的。高脂血症患者一年仅需注射2针inclisiran,就能显著和持久地降低LDL-C,而其安全性与安慰剂近似,这势必将再掀起一股针对PCSK9靶点的基因治疗药物的研发热潮。
PCSK9人源化小鼠构建
集萃药康通过基因编辑技术,将鼠源PCSK9相应片段原位替换为人源片段,构建出PCSK9人源化小鼠,针对RNAi类药物的开发需求还进一步开发了包含3’UTR区的新型PCSK9人源化小鼠。PCSK9人源化小鼠经西方饮食饲料(Western Diet)诱导可出现高胆固醇血症表型,满足心血管疾病研究及相关治疗药物评价的需求。
B6-hPCSK9人源化小鼠信息
品系编号 | 品系名称 | 品系背景 | 人源化区域 | 应用 |
C57BL/6JGpt | CDS | 降血脂研究,心血管疾病研究; | ||
C57BL/6JGpt | CDS+3’UTR | 降血脂研究,心血管疾病研究; |
B6-hPCSK9-UTR小鼠药效验证(Inclisiran)
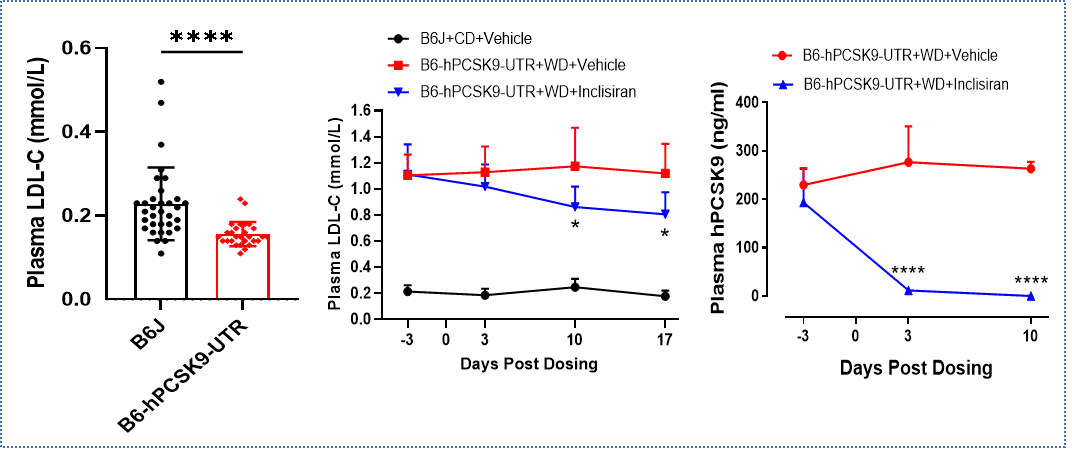
6周龄B6-hPCSK9-UTR小鼠血液中LDL-C水平略低于野生型C57BL/6J小鼠。单次皮下注射Inclisiran可显著降低WD喂养的B6-hPCSK9-UTR小鼠血液中的LDL-C水平以及hPCSK9水平。
参考文献:
1. Goldstein, J. L. & Brown, M. S. The LDL receptor. Arteriosclerosis, thrombosis, and vascular biology. 29, 431-438, doi:10.1161/ATVBAHA.108.179564(2009).
2. Huang, S., Henry, L., Ho, Y. K., Pownall, H. J. & Rudenko, G.Mechanism of LDL binding and release probed by structure-based mutagenesis of the LDL receptor. Journal of lipid research. 51, 297-308, doi:10.1194/jlr.M000422 (2010).
3. Horton, J. D., Cohen, J. C. & Hobbs, H. H. Molecular biology of PCSK9: its role in LDL metabolism. Trends in biochemical sciences. 32, 71-77, doi:10.1016/j.tibs.2006.12.008 (2007).
4. Lin, X. L., Xiao, L. L., Tang, Z. H., Jiang, Z. S. & Liu, M. H. Role of PCSK9 in lipid metabolism and atherosclerosis. Biomed Pharmacother.104, 36-44, doi:10.1016/j.biopha.2018.05.024 (2018).
5. Seidah, N. G., Awan, Z., Chretien, M. & Mbikay, M. PCSK9: a key modulator of cardiovascular health. Circulation research. 114, 1022-1036, doi:10.1161/CIRCRESAHA.114.301621 (2014).
6. Abifadel, M. et al. Identification and characterization of new gain-of-function mutations in the PCSK9 gene responsible for autosomal dominant hypercholesterolemia. Atherosclerosis. 223, 394-400, doi:10.1016/j.atherosclerosis.2012.04.006 (2012).
7. Carreras, A. et al. In vivo genome and base editing of a human PCSK9 knock-in hypercholesterolemic mouse model. BMC biology. 17, 4, doi:10.1186/s12915-018-0624-2(2019).
8. Rashid, S. et al. Decreased plasma cholesterol and hypersensitivity to statins in mice lacking Pcsk9. Proc Natl Acad Sci U S A. 102, 5374-5379, doi:10.1073/pnas.0501652102(2005).