特应性皮炎(atopic dermatitis, AD)又称特应性湿疹,是一种易复发、瘙痒性的炎症性皮肤病,是皮肤科最常见的疾病之一,发病率高且难以根治。通常初发于婴儿期,儿童患病率高达20%,也可发于成人。疾病最主要的特征是皮肤干燥、反复发作的皮肤瘙痒及湿疹,使患者陷入“越抓越痒”的恶性循环。此外患者往往合并其他全身过敏性疾病,如过敏性鼻炎、哮喘等[1],因此也常被称为“过敏三姐妹”。
图1.AD疾病主要表型(来源于网络)
AD病因及发病机制复杂,目前尚未完全明确。但AD发病的诱因一般认为与遗传、环境因素、皮肤屏障功能障碍、微生物失调、免疫失调及皮肤炎症与环境间的互作存在密切的关系。AD发病的首要特征是皮肤屏障的改变和外界抗原的入侵[1],破坏表皮屏障后,接着会引起表皮免疫系统失调,其中,Th2细胞的激活被认为是AD炎症表型的最主要通路,活化的Th2细胞释放大量相关炎性因子促进炎症的产生,进一步削弱皮肤屏障功能[2,3]。
AD目前尚无根治方法,临床治疗目标主要以缓解症状,提高患者生存质量为主。除了传统的使用保湿剂、糖皮质激素及免疫抑制剂外,近几年来,不少新兴的疗法层出不穷,如抗白细胞介素(IL-4R)的度普利尤单抗和抗免疫球蛋白(IgE )的奥马珠单抗;同时,多款JAK抑制剂如巴瑞替尼、乌帕替尼、阿布昔替尼也被应用于特应性皮炎的治疗当中;此外一些外用的药物如克立硼罗软膏也已在中国上市,为特应性皮炎患者的治疗提供更多选择。
从目前的临床治疗效果来看,现有的治疗手段仍存在一定局限性。传统药物使用频率较广,但局部使用对于中、重度患者效果有限;生物制剂类药物有显著改善的效果,但也存在临床研究结果有限的情况,并表现出个体差异性,因此发展新型且安全有效的治疗方法是十分必要的。值得一提的是,除了现有已上市及处于临床试验阶段的靶点外,仍有很多潜在的创新型靶点和策略为特应性皮炎药物开发提供新的思路,同时,针对不同亚型特应性皮炎患者的个体化治疗和研究也在进行中,无疑推动了AD的精准诊疗。
无论是小分子药物,还是针对创新型靶点的抗体药,亦或是微生物疗法,都需要进行严谨的临床前体内研究,一个合适的动物模型无疑成为药物研发过程中不可或缺的一部分。集萃药康凭借丰富的模型构建经验,已成功构建了多种AD动物模型,针对不同药物的作用机制可匹配不同的模型,用于药物研发阶段有效性验证。

MC903即卡泊三醇,是一种维生素D3的低钙类似物,广泛用于治疗银屑病。研究发现,局部使用MC903可激发小鼠上皮角质细胞高表达TSLP,促进CD4+T细胞向Th2细胞分化及激活并释放炎症细胞因子,引起小鼠产生特应性皮炎表型。
数据展示
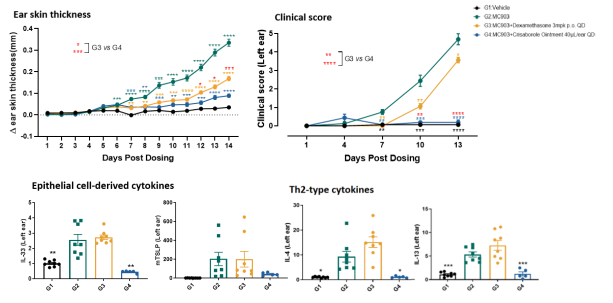
图2.使用克立硼罗软膏可明显降低MC903诱导的AD模型组小鼠皮肤厚度及疾病评分,以及细胞因子的水平。
恶唑酮(Oxazolone,OXA)与1,2,4-二硝基氟苯(1,2,4-Dinitrofluorobenzene,DNFB)等化合物属于半抗原,能与皮肤组织蛋白结合成为完全抗原,进而激活T淋巴细胞实质成为致敏细胞,当半抗原再次进入机体,与致敏淋巴细胞接触就会引发过敏反应[4]。
数据展示
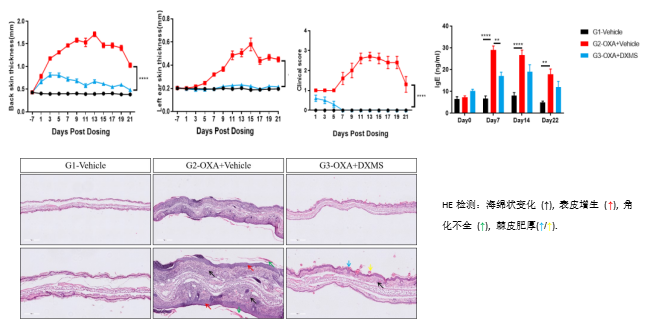
图3.使用地塞米松显著降低OXA诱导AD模型组小鼠皮肤厚度及疾病评分,以及IgE抗体水平。
数据展示
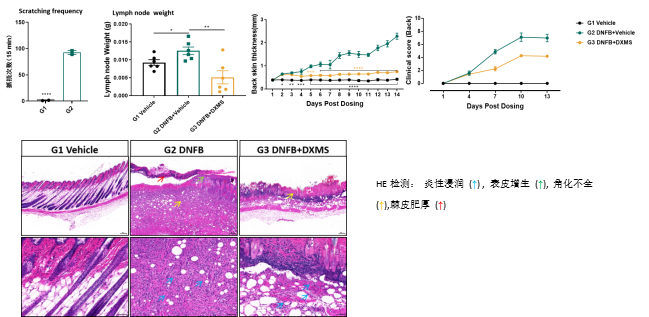
图4.模型组瘙痒频率加大提高,皮肤变厚,病理病变严重,使用地塞米松后能有效缓解疾病表型。
集萃药康自免平台可提供动物模型和技术服务,并可定制药物开发临床前一站式服务,主要聚焦系统性红斑狼疮、炎性肠病、多发性硬化症、银屑病、特应性皮炎、类风湿性关节炎等疾病领域。
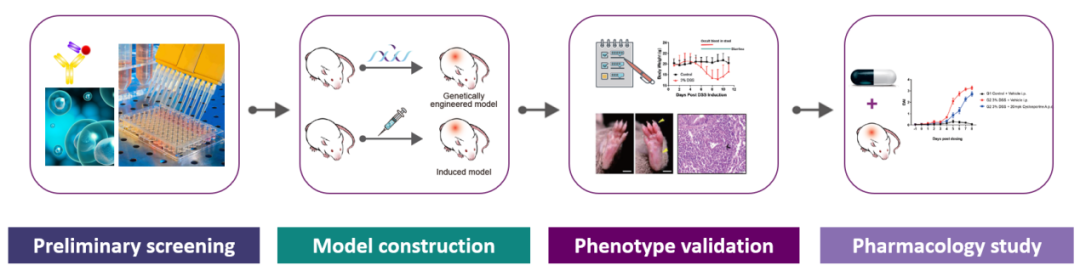
自免药物临床前一站式服务
参考资料
[1]Weidinger, S. and N. Novak, Atopic dermatitis. The Lancet, 2016. 387(10023): p. 1109-1122.
[2]Nutten, S., Atopic dermatitis: global epidemiology and risk factors. Annals of nutrition & metabolism. 66 Suppl 1: p. 8-16.[3]Nutten, S., Atopic dermatitis: global epidemiology and risk factors. Annals of nutrition & metabolism. 66 Suppl 1: p. 8-16.
[3]李覃,高颖,曹波,等.变态反应性接触性皮炎体内外模型制作探讨[J].武警医学, 2013,24(10):849-852.