PDXモデル(Patient-Derived tumor Xenograft model)は、ヒト由来腫瘍異種移植であり、主に患者の新鮮な腫瘍組織を免疫不全マウス(NCGなど)に移植することによって構築されます。このモデルは、患者の腫瘍の元の生物学的特徴、病理学的タイピング、分子マーカー発現、遺伝子変異タイプなどをより完全に維持することができます。

薬康の優位性
集萃薬康が独自で開発したNCGマウスはゲノム編集技術を使用してNOD/ShiltJGptマウスのPrkdc及びIl2rg遺伝子をノックアウトすることで得られた重度免疫不全系統です。NCGマウスは、T細胞、B細胞、NK細胞が欠失していることを特徴としており、これまでの免疫系欠損症の最も完全なマウスモデルであり、PDXモデルの構築や薬物学的スクリーニングに非常に適しています。
集萃薬康は、独立した知的財産権を持っている複数種類のPDXモデルリソースを構築し、膵臓がん、結腸がん、乳がん、肺がんなどを含む複数種類の一般的な臨床悪性腫瘍をカバーし、PDXの薬物学的評価に用いています。
集萃薬康は、PDX薬物スクリーニングのガイダンスを提供するために、多数のPDXモデルシーケンスおよび表面マーカー分析などの作業を実行しました。
業務詳細
PDXモデルリソース

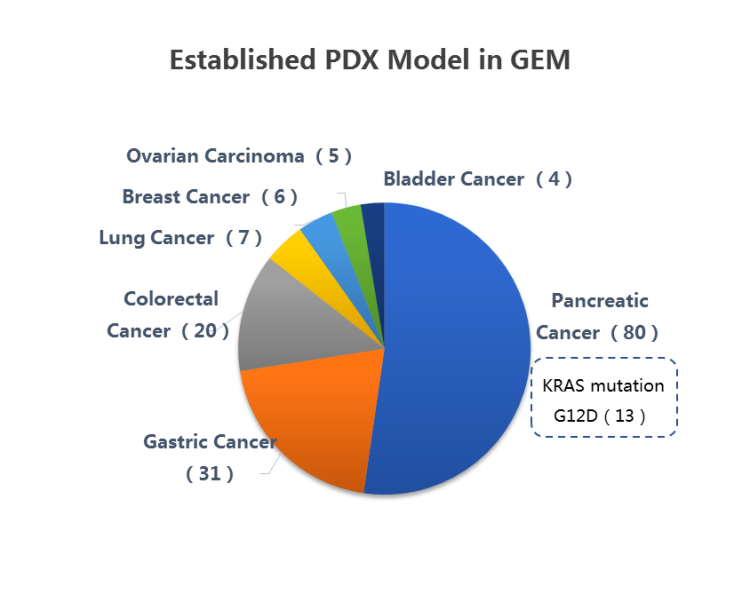
PDXモデリングおよび病理学的分析:
Case1:胃がん(手術サンプル)PDXモデル
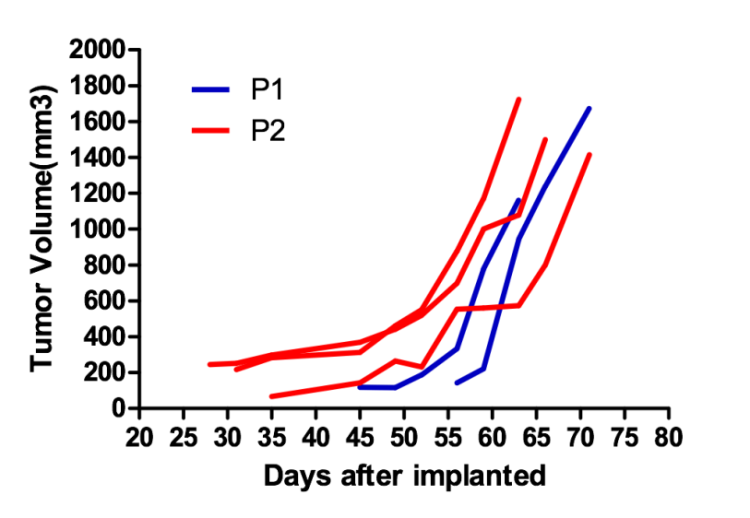
図1-1. NCGマウスのインビボPDX腫瘍増殖曲線。
P1:患者の腫瘍組織をNCGマウス体内に接種して増殖させた第1世代モデル;P2:P1世代の腫瘍モデルを他のNCGマウス体内に継代させた第2世代モデル。

図1-2. PDXモデル腫瘍組織HE染色画像の比較。
PDX標本は、臨床腫瘍標本の特異的腺管様構造を保持しています。P0:患者の腫瘍組織のHE染色画像。P2:PDX第2世代腫瘍標本のHE染色画像。
Case2:結腸癌肝転移(パンクチャーサンプル)のPDXモデル

図2-1. NCGマウスのインビボPDX腫瘍増殖曲線。
P1:患者の腫瘍組織をNCGマウスに接種して増殖させた第1世代モデル;P2:P1世代の腫瘍モデルを他のNCGマウス体内に継代させた第2世代モデル。パンクチャーサンプル量が少なく、増殖速度が遅いため、P2世代の増殖速度が有意に上がりました。
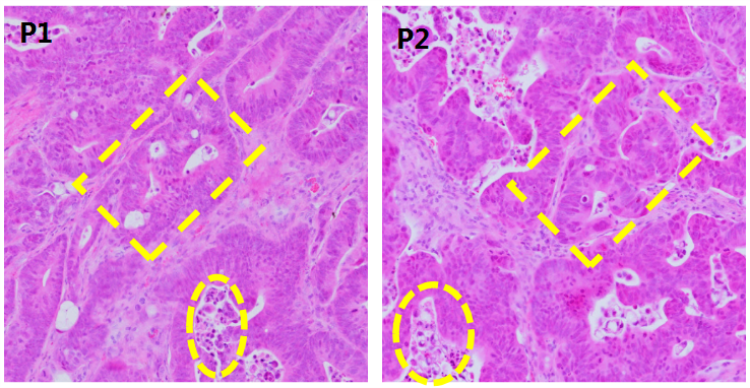
図2-2. PDXモデル腫瘍組織HE染色画像の比較。
PDX標本の世代間において、高度に分裂した細胞タイプが保持されました。
PDXの薬効事例
Case1:膵臓がんにおけるPDXの薬効

図1-1. 膵臓がんにおけるPDX(P2)薬効グループ化後の腫瘍増殖曲線(Mean±SEM)
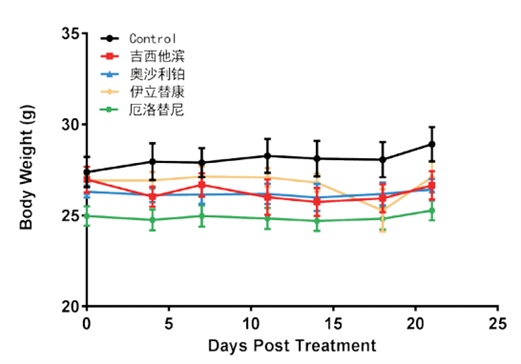
図1-2. 膵臓がんにおけるPDX(P2)の薬効グループ化後のマウス体重曲線(Mean±SEM)
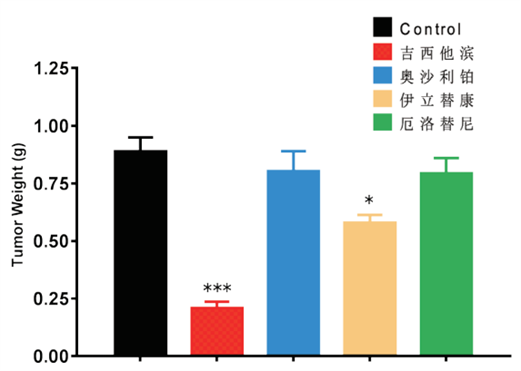
図1-3. 膵臓癌PDX(P2)の薬効エンドポイント処理腫瘍重量(Mean±SEM)
*:0.01≤P<0.05,**:0.001≤P<0.01 vs 対照群(Control)、ポストホックテストはDunnettです。対照群G1と比較して、ゲムシタビン治療群、イリノテカン治療群の腫瘍重量はいずれも有意に減少しました。
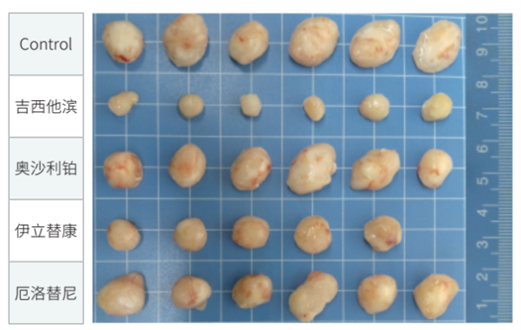
図1-4. 膵臓がんPDX(P2)の薬効エンドポイント処理の腫瘍写真
グループ | 治療方法 | TGI on D21 | P value on D21 |
G2 | 吉西他滨 ゲムシタビン | 90.34% | 0.008** |
G3 | 奥沙利铂 オキサリプラチン | 44.95% | 0.215 |
G4 | 伊立替康 イリノテカン | 67.85% | 0.026* |
G5 | 厄洛替尼 エルロチニブ | 52.59% | 0.073 |
表1-2.各群の薬剤による腫瘍増殖阻害率TGIおよび統計分析。
*:0.01≤P<0.05,**:0.001≤P<0.01 vs 対照群(Control)。対照群と比較して、G2、G4群のエンドポイント治療当日のD21の腫瘍体積には有意な統計的差異が認められました。
Case2:骨肉腫におけるPDXの薬効
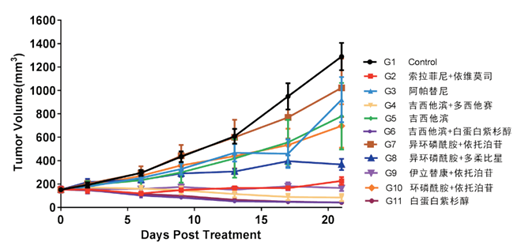
図2-1. 骨肉腫PDX(P2)の薬効グループ化後の腫瘍増殖曲線(Mean±SEM)
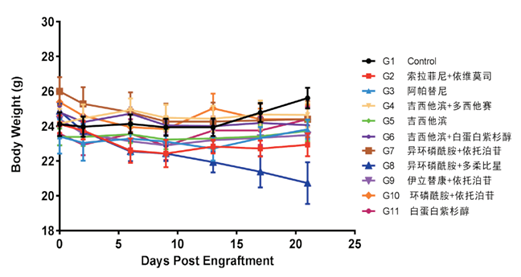
図2-2. 骨肉腫におけるPDX(P2)の薬効グループ化後のマウス体重変化(Mean±SEM)
その中で、G8群のマウスの体重は有意に減少し(*:0.01≤P<0.05)、他の群と対照群の間に有意差は認められません

図2-3.骨肉腫PDX(P2)の薬効エンドポイント治療腫瘍重量(Mean±SEM)
**:0.001≤P < 0.01,***:P < 0.001 VS対照群(Control)、ポストホックテストはDunnettです。対照群G1と比較して、G2、G4、G6、G8、G9、およびG11群の腫瘍重量は有意に減少しました。

図2-4. 骨肉腫PDXの薬効エンドポイントの腫瘍写真
グループ | 治療方法 | TGI on D21 | p value |
G2 | 索拉菲尼+依维莫司 ソラフェニブ+エベロリムス | 86.10% | 0.004** |
G3 | 阿帕替尼 アパチニブ | 28.58% | 0.949 |
G4 | 吉西他滨+多西他赛 ゲムシタビン+ドセタキセル | 93.49% | 0.002** |
G5 | 吉西他滨 ゲムシタビン | 39.54% | 0.942 |
G6 | 吉西他滨+白蛋白紫杉醇 ゲムシタビン+アルブミンパクリタキセル | 96.73% | 0.002** |
G7 | 异环磷酰胺+依托泊苷 イホスファミド+エトポシド | 20.69% | 1 |
G8 | 异环磷酰胺+多柔比星 イホスファミド+ドキソルビシン | 39.88% | 0.006** |
G9 | 伊立替康+依托泊苷 イリノテカン+エトポシド | 87.17% | 0.003** |
G10 | 环磷酰胺+依托泊苷 シクロホスファミド+エトポシド | 45.99% | 0.478 |
G11 | 白蛋白紫杉醇 アルブミンパクリタキセル | 96.75% | 0.003** |
表2-2. 各群の薬剤による腫瘍増殖阻害率TGIおよび統計分析。
**:0.001≤P < 0.01,***:P < 0.001 VS対照群(Control)、ポストホックテストはDunnettです。対照群と比較して、G2、G4、G6、G8、G9、およびG11群のエンドポイント治療当日のD21の腫瘍体積には有意な統計的差異が認められました。